Plateforme ARN
Le travail pionnier de Sarepta sur la chimie des oligomères de morpholino de phosphorodiamidate (phosphorodiamidate morpholino oligomer, PMO) est à la base de nos thérapies de saut d’exon.
Notre chimie de nouvelle génération s’appelle oligomères Peptide-conjugués de morpholino (Peptide-Conjugated Phosphorodiamidate Morpholino Oligomer, PPMO), car cela permet d’ajouter un peptide à la structure du PMO, dans le but d’augmenter la pénétration des noyaux cellulaires, et a le potentiel d’élargir notre portefeuille thérapeutique.
L’ARN et son rôle dans la maladie génétique
Les origines des maladies neuromusculaires héréditaires et des maladies du système nerveux central peuvent presque toujours être liées à des mutations génétiques qui interfèrent avec la production de protéines critiques.
Les gènes sont des segments d’ADN et ils se trouvent dans presque toutes les cellules de l’organisme. Lorsque l’organisme a besoin de fabriquer une protéine, les informations contenues dans l’ADN sont transmises à une molécule similaire appelée ARN. À terme, une forme d’ARN appelée ARN messager (ARNm) transmet les instructions à une particule dans la cellule qui utilise les instructions pour assembler la protéine. Une maladie génétique survient lorsqu’une mutation est transmise à l’ARN messager, créant une erreur dans les instructions nécessaires pour produire une certaine protéine.
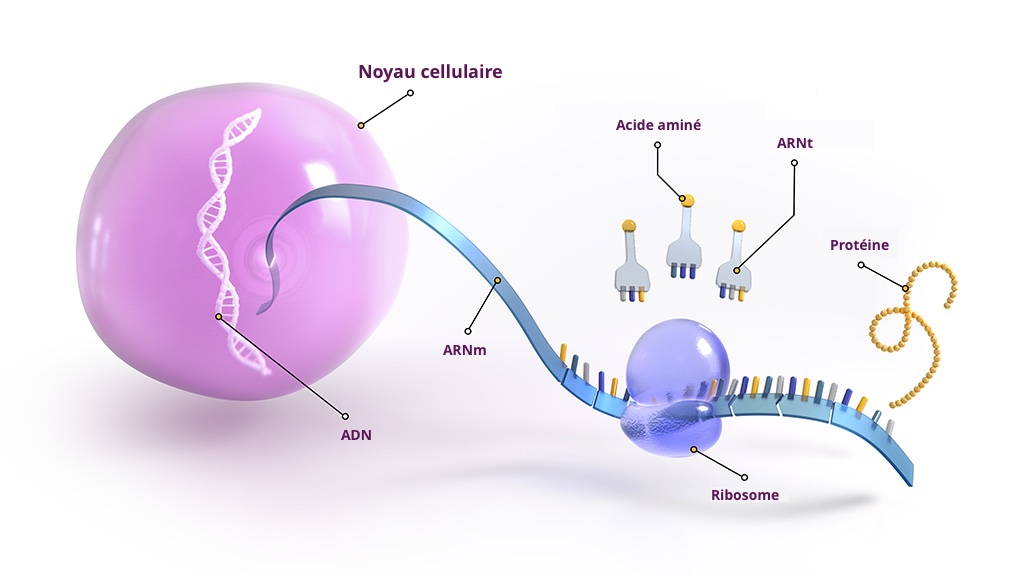
Technologies ARN : PMO et PPMO
PMO :
Les oligomères de morpholino de phosphorodiamidate, ou PMO, sont des molécules synthétiques prenant pour modèle le cadre naturel de l’ARN. Alors que les PMO contiennent les mêmes bases d’acides nucléiques retrouvées dans l’ARN, ils sont liés à des cycles morpholine à six côtés au lieu de cycles ribose à cinq côtés. En outre, les cycles morpholine sont connectés les uns aux autres par des liaisons phosphorodiamidate au lieu des liaisons phosphodiester retrouvées dans l’ARN. Cela permet aux PMO de se lier à des séquences spécifiques d’ARN pré-messager tout en restant hautement résistants à la dégradation.
PPMO
Les oligomères Peptide-conjugués de morpholino, ou PPMO, sont des thérapies exclusives de nouvelle génération à base de PMO de Sarepta en développement et sont spécifiquement conçus pour augmenter la pénétration tissulaire par rapport aux PMO. Des études non cliniques ont démontré une administration ciblée dans les cellules squelettiques, cardiaques et musculaires lisses et une augmentation ultérieure de la modification de l’ARNm. L’objectif de ces programmes de développement est d’apprendre si l’ajout du peptide peut améliorer l’efficacité et réduire la posologie, en plus d’élargir l’éventail des maladies qu’il peut traiter.
Saut d’exon
De nombreuses maladies sont causées par une mutation génétique dans un gène particulier. Le plus souvent, un ou plusieurs exons (parties du gène) sont absents, ce qui provoque des erreurs dans les instructions de fabrication d’une protéine spécifique. Cela se traduit par une incapacité de l’organisme à produire la protéine en quantité suffisante, voire à n’en produire aucune. Le but du saut d’exon est d’agir sur l’ARN pour permettre à l’organisme de produire une version de la protéine manquante pour contourner la mutation.
Exemple de saut d’exon
Un gène est composé d’exons (portions d’un gène) qui sont liés ensemble pour fournir des instructions en vue de fabriquer une protéine spécifique.
Chaque exon se connecte à ses exons voisins d’une manière spécifique. L’exon 43, par exemple, se connecte d’un côté à l’exon 42 d’une manière spécifique et de l’autre à l’exon 44, également d’une manière spécifique.
Si l’exon 43 est absent, l’exon 42 ne peut pas se connecter directement à l’exon 44 car leurs connecteurs ne s’emboîtent pas et, du fait qu’ils ne s’emboîtent pas, l’organisme est incapable de lire les instructions génétiques pour fabriquer la protéine.
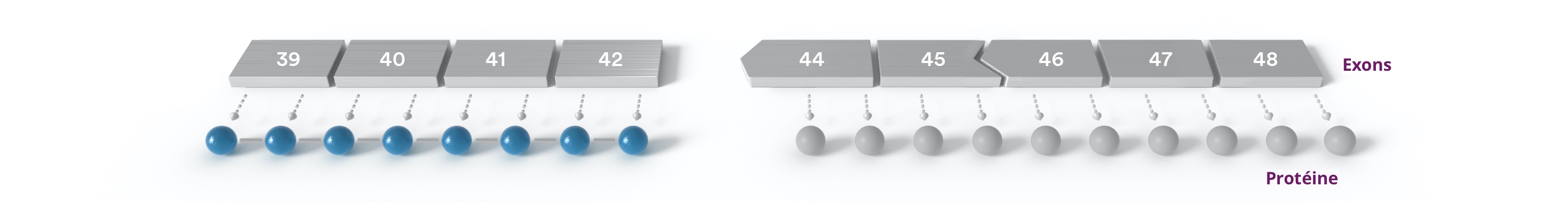
Sauter des exons
En masquant certains exons, on peut « sauter » leur emplacement pour se lier à un exon avec le bon connecteur. Cela permettrait une production d’une forme raccourcie et potentiellement fonctionnelle de la protéine manquante.
Dans cet exemple, le PMO dirige les mécanismes d’épissage pour sauter un exon lors du traitement du pré-ARNm. Par conséquent, l’ARNm alternatif permet la production d’une forme plus courte de la protéine manquante. 
