RNA-Plattform
Die wegweisende Arbeit von Sarepta mit den Phosphorodiamidat-Morpholino-Oligomer (PMO)-Stoffen ist die Grundlage unserer Exon-Skipping-Therapien.
Unsere Chemie der nächsten Generation heißt PPMO, weil sie der PMO-Struktur ein Peptid hinzufügt, mit dem Ziel, die Zellkernpenetration zu erhöhen, und das Potenzial hat, unser therapeutisches Portfolio zu erweitern.
RNA und ihre Rolle bei genetischen Erkrankungen
Der Ursprung von vererbten neuromuskulären Erkrankungen und Erkrankungen des zentralen Nervensystems kann fast immer auf genetische Mutationen zurückgeführt werden, die die Produktion kritischer Proteine beeinträchtigen.
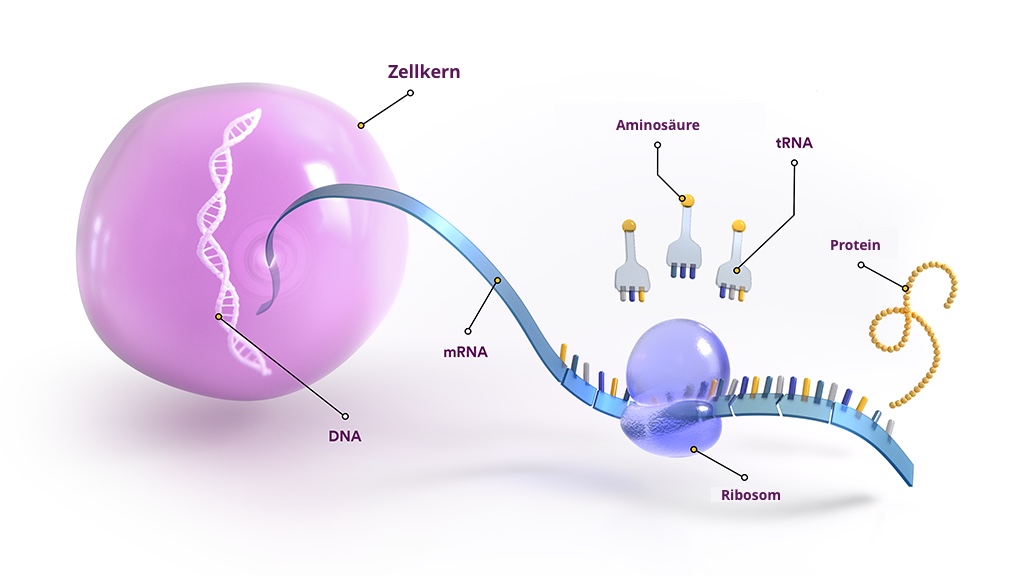
Gene sind DNA-Segmente, die sich in fast jeder Zelle im Körper finden. Wenn der Körper ein Protein herstellen muss, werden Informationen in der DNA an ein ähnliches Molekül weitergegeben, das als RNA bekannt ist. Letztendlich gibt eine Form der RNA, die als Messenger-RNA (mRNA) bezeichnet wird, die Anweisungen an ein Partikel in der Zelle weiter, das die Anweisungen zur Zusammenstellung des Proteins verwendet. Eine genetische Störung tritt auf, wenn eine Mutation an die Messenger-RNA weitergegeben wird, wodurch ein Fehler in der Anweisung entsteht, die zur Produktion eines bestimmten Proteins erforderlich ist.
RNA-Technologien: PMO und PPMO
PMOs
Phosphorodiamidat-Morpholino-Oligomere oder PMOs sind synthetische Moleküle, die nach dem natürlichen Rahmen der RNA modelliert sind. Während PMOs die gleichen Nukleinsäurebasen wie RNA haben, sind sie an sechsseitige Morpholinringe statt an fünfseitige Ribose-Ringe gebunden. Zusätzlich sind die Morpholinringe durch Phosphorodiamidatbindungen anstelle der in der RNA vorkommenden Phosphodiesterbindungen miteinander verbunden. Dies ermöglicht es PMOs, sich an spezifische RNA-Sequenzen vor dem Messenger zu binden, während sie hochresistent gegen den Abbau bleiben.
PPMOs
Peptid-Phosphorodiamidat-Morpholino-Oligomere, oder PPMOs, sind die proprietären PMO-basierten Therapien der nächsten Generation von Sarepta in der Entwicklung und wurden speziell entwickelt, um die Gewebepenetration im Vergleich zu PMOs zu erhöhen. Nichtklinische Studien haben eine gezielte Abgabe an Skelett-, Herz- und glatte Muskelzellen und eine nachfolgende erhöhte mRNA-Modifikation gezeigt. Das Ziel dieser Entwicklungsprogramme ist es, zu erfahren, ob die Zugabe des Peptids die Wirksamkeit verbessern und die Dosierung reduzieren kann, zusätzlich zur Erweiterung des Spektrums der Krankheiten, die behandelt werden können.
Exon-Skipping
Viele Krankheiten werden durch eine genetische Mutation in einem bestimmten Gen verursacht. Am häufigsten fehlen ein oder mehrere Exons (Teile des Gens), was zu Fehlern in den Anweisungen zur Herstellung eines bestimmten Proteins führt. Dies führt dazu, dass der Körper nicht in der Lage ist, genug dieses Proteins – oder dieses Protein überhaupt – herzustellen. Das Ziel des Exon-Skippings besteht darin, auf die RNA zu wirken, damit der Körper eine Version des fehlenden Proteins herstellen kann, um die Mutation zu umgehen.
Ein Beispiel für Exon-Skipping
Ein Gen besteht aus Exonen (Teilen eines Gens), die miteinander verbunden sind, um Anweisungen zur Herstellung eines spezifischen Proteins zu geben.
Jedes Exon verbindet sich auf eine bestimmte Weise mit seinen benachbarten Exons. Exon 43 verbindet sich beispielsweise auf einer Seite auf eine bestimmte Weise mit Exon 42 und auf der anderen – auch auf eine bestimmte Weise – mit Exon 44.
Wenn Exon 43 fehlt, kann Exon 42 nicht direkt mit Exon 44 verbunden werden, weil ihre Konnektoren nicht zusammenpassen und darum kann der Körper die genetischen Anweisungen zur Herstellung des Proteins nicht lesen.
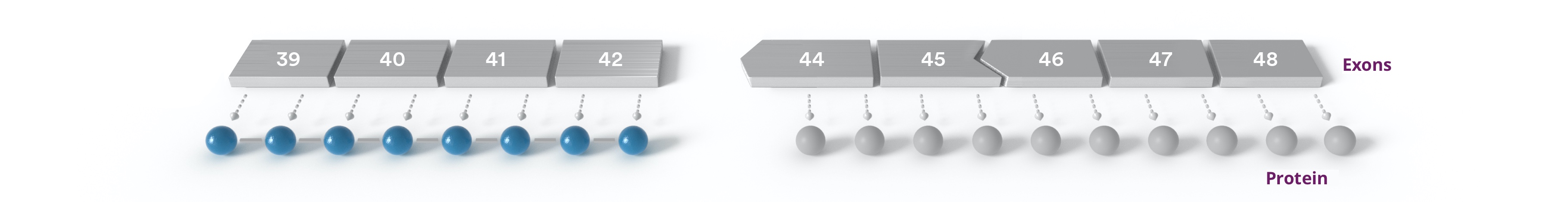
Überspringen von Exons
Durch das Ausblenden bestimmter Exons können wir deren Lage "überspringen", um mit einem Exon mit dem richtigen Konnektor in Verbindung zu treten. Dies würde die Produktion einer verkürzten und potenziell funktionellen Form des fehlenden Proteins ermöglichen.
In diesem Beispiel weist der PMO den Spleiss-Mechanismus an, bei der Verarbeitung der Pre-mRNA ein Exon zu überspringen. Dadurch ermöglicht die alternative mRNA die Produktion einer kürzeren Form des fehlenden Proteins. 
